คลิกที่น - โรงเรียนมหิดลวิทยานุสรณ์
advertisement

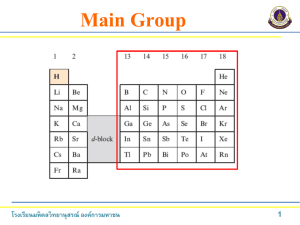
Inorganic Chemistry Aj. Chatuporn Sawatruksa Department of Chemistry Room 3501 Chatupornsawatdee@gmail.com Facebook: Chatuporn sawatruksa 08-6528-9482 Periodic table • วิวัฒนาการตารางธาตุ และแนวโน้ มตามตารางธาตุ • สมบัตทิ างกายภาพ ปฏิกริ ิยาเคมี และสารประกอบ ของธาตุหมู่ 1, 2 ของธาตุกลุ่ม s-block โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 2 Periodic Table โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 3 โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 4 • วิวัฒนาการตารางธาตุ และแนวโน้ มตามตารางธาตุ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 5 1817 Johann Dobereiner Li Na K (7 + 39) ÷ 2 = 23 7 23 39 Ca Sr Ba (40 + 137) ÷ 2 = 88 40 88 137 But Cu Ag 63.6 108 โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน Au 197 จัดธาตุเป็ นหมวดหมูๆ่ ละ 3 ธาตุ ตามสมบัติที่คล้ ายคลึงกัน เรี ยกว่า triads โดยธาตุตวั กลางจะมีน ้าหนัก อะตอมเป็ นค่าเฉลี่ยของน ้าหนัก อะตอมของธาตุที่เหลือกฎนี ้เรี ยกว่า Law of Triads (63.6 + 197) ÷ 2 = 130.3 6 1864 John Newlands Li Be B C N O F Na Mg Al Si P S Cl K Ca Cr Ti Mn Fe Co,Ni Cu Zn Y In As Se Br Law of Octaves ถ้ านาธาตุมาเรี ยงลาดับตามน ้าหนักอะตอม จะพบว่า ธาตุ ตัวที่ 8 จะมีสมบัติคล้ ายธาตุตวั ที่ 1 โดยเริ่มจากธาตุใดก็ได้ ไม่รวม ไฮโดรเจน กับแก๊ สมีตระกูล * กฎนี ้ใช้ ได้ กบั ธาตุที่มีน ้าหนักอะตอมไม่เกินน ้าหนักอะตอมของแคลเซียม โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 7 1869-1870 Julius Lothar Meyer and Dmitri Ivanovich Mendeleev ถ้ าเรี ยงตามน ้าหนักอะตอมจากน้ อยไปหามาก แล้ ว แบ่งเป็ นแถวให้ เหมาะสม ธาตุที่มีสมบัติทางเคมีและ กายภาพคล้ ายกันจะปรากฎอยูต่ รงกันเป็ นช่วงๆ สมบัติของธาตุตา่ งๆ เป็ นฟั งก์ชนั พิริออดิกของน ้าหนัก อะตอมของธาตุเหล่านัน้ เรี ยกว่า Periodic Law โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 8 ตารางธาตุฉบับแรกของเมนเดเลเอฟ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 9 ตาราง เปรียบเทียบสมบัตขิ องธาตุเอคาซิลิคอนกับเจอร์ เมเนียมที่ทานายและที่ค้นพบ เอคาซิลิคอนทานาย เจอร์ เมเนียมพบเมื่อ เมื่อ พ.ศ. 2414 พ.ศ. 2429 (ค.ศ.1886) (ค.ศ. 1871) มวลอะตอม 72 72.6 สีของธาตุ เป็ นโลหะสีเทา เป็ นโลหะสีเทา ความหนาแน่ น (g/cm3) 5.5 5.36 จุดหลอมเหลว (0C ) สูง 958 สูตรของออกไซด์ GeO2 GeO2 ความหนาแน่ นของออกไซด์ (g/cm3) 4.7 4.70 เมื่อผสมกับกรดไฮโดรคลอริก ละลายได้ เล็กน้ อย ไม่ ละลายที่ 25 0C สมบัติ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 10 1913 Henry G.J. Moseley ต าแหน่ ง ของธาตุ ใ นตารางธาตุ น่ า จะขึ น้ อยู่ กั บ สมบั ติ อื่ นที่ มี ความสัมพันธ์กบั น ้าหนักอะตอม นัน่ คือ เลขอะตอม Periodic Law มีความหมายว่ า “สมบัติต่าง ๆ ของธาตุจะ ขึน้ อยู่กับเลขอะตอมของธาตุนัน้ และขึน้ อยู่กับการจัดอิเล็กตรอน ของธาตุเหล่ านัน้ ” โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 11 Gallium arsenide (GaAs) ekaaluminium As Ga (จากภาษาละติน Gallia แปลว่ า ฝรั่ งเศส) ใช้ เป็ นแหล่งกาเนิดแสง เลเซอร์ ในเครื่ องเล่นซีดี โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 12 Periodic Table โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 13 ตารางธาตุในปั จจุบนั Periodic Table p-BLOCK ns2np1-6 d-BLOCK s-BLOCK ns1, ns2 f-BLOCK s-block p-block โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน d-block f-block 15 การตั้งชื่อธาตุทคี่ ้ นพบใหม่ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 16 การตั้งชื่อธาตุทคี่ ้ นพบใหม่ การตังชื ้ ่อธาตุที่ค้นพบในยุคแรกจะใช้ ชื่อนักวิทยาศาสตร์ ที่ค้นพบ ธาตุบางธาตุถกู ค้ นพบโดยนักวิทยาศาสตร์ หลายคณะ ทาให้ มีชื่อเรี ยกและสัญลักษณ์ต่างกัน โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 17 การตั้งชื่อธาตุทคี่ ้ นพบใหม่ การที่คณะนักวิทยาศาสตร์ ตา่ งคณะตังชื ้ ่อแตกต่างกัน ทาให้ เกิดความสับสน International Union of Pure and Applied Chemistry (IUPAC) จึงได้ กาหนด ระบบการตังชื ้ ่อขึ ้นใหม่ โดยใช้ กบั ชื่อธาตุที่มีเลขอะตอมเกิน 100 ขึ ้นไป ทังนี ้ ้ให้ ตังชื ้ ่อธาตุโดยระบุเลขอะตอมเป็ นภาษาละติน แล้ วลงท้ ายด้ วย -ium ระบบการนับเลขในภาษาละตินเป็ นดังนี ้ 0 = nil (นิล) 2 = bi (ไบ) 4 = quad (ควอด) 6 = hex (เฮกซ์) 8 = oct (ออกตฺ) โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 1 3 5 7 9 = = = = = un (อุน) tri (ไตร) pent (เพนท์) sept (เซปท์) enn (เอนน์) 18 การตั้งชื่อธาตุทคี่ ้ นพบใหม่ ตัวอย่างที 1่ จงอ่านชื่อตามระบบ IUPAC พร้ อมทังเขี ้ ยนสัญลักษณ์ของธาตุตอ่ ไปนี ้ 1. ธาตุที่ 106 =________________________________สัญลักษณ์___________ 2. ธาตุที่ 208 =________________________________สัญลักษณ์___________ 3. ธาตุที่ 119 =________________________________สัญลักษณ์___________ 4. ธาตุที่ 135 =________________________________สัญลักษณ์___________ 5. ธาตุที่ 374 =________________________________สัญลักษณ์___________ ตัวอย่างที 2่ ธาตุที่มีสญ ั ลักษณ์ตอ่ ไปนี ้มีเลขอะตอมเท่าไร 1. Unh =________________ 2. Uno =_________________ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 19 แนวโน้ มของสมบัตติ ามตารางธาตุ แนวโน้ มของสมบัตทิ างกายภาพ 1. ขนาดอะตอม 2. รั ศมีไอออน 3. พลังงานไอออไนเซชัน 4. อิเล็กโตรเนกาติวิตี 5. สัมพรรคภาพอิเล็กตรอน 6. จุดเดือดจุดหลอมเหลว โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 20 ขนาดอะตอม ธาตุในคาบเดียวกัน เมื่อเลขอะตอมเพิ่มขึ ้น ขนาดอะตอมจะเล็กลง เนื่องจากธาตุในคาบ เดียวกันมีจานวนระดับพลังงานเท่ากัน แต่เมื่อเลขอะตอมเพิ่ม จานวนโปรตอนจะเพิ่มขึ ้นด้ วย แรงดึงดูดระหว่างนิวเคลียสกับเวเลนซ์อิเล็กตรอนเพิ่มขึ ้น ขนาดจึงลดลง ธาตุใ นหมู่ เ ดี ย วกัน เมื่ อ เลข อะตอมเพิ่มขึ ้น ขนาดอะตอม จะใหญ่ ขึ น้ เพราะเมื่ อ เลข อะตอมเพิ่ ม ขึน้ จะมี จ านวน ระดับพลังงานเพิ่มขึน้ แม้ ว่า จ านวนโปรตอนจะเพิ่ ม ขึ น้ ด้ ว ยก็ ต าม แต่ แ รงดึง ดูด ต่ อ เวเลนซ์อิเล็กตรอนมีน้อย จึง ทาให้ ขนาดใหญ่ขึ ้น กล่าวได้ ว่ า ก ร ณี นี ก้ า ร เ พิ่ ม ร ะ ดั บ พลัง งานมี ผ ลมากกว่ า การ เพิ ่มจยานวนโปรตอน โรงเรี นมหิดลวิทยานุสรณ์ องค์การมหาชน 21 รัศมีไอออน Mg : 1s2 2s2 2p6 3s2 160 pm รัศมีไอออน คือระยะระหว่างนิวเคลียสของไอออนคู่ หนึ่งๆ ที่มีแรงยึดเหนี่ยวซึง่ กันและกันในโครงผลึก Mg2+ : 1s2 2s2 2p6 65 pm O : 1s2 2s2 2p4 73 pm โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน O2- : 1s2 2s2 2p6 140 pm 22 “ไอออนของโลหะ ในหมู่เดียวกันจะมี ขนาดใหญ่ขึ้นเมื อ่ เลขอะตอม เพิ่ มขึ้น” และ “ไอออนของโลหะ ในคาบเดียวกันจะ มีขนาดเล็กลงเมื อ่ เลขอะตอม เพิ่ มขึ้น” โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน ขนาดไอออน “ไอออนของ อโลหะในหมู่ เดียวกัน จะมี ขนาดใหญ่ขึ้น เมือ่ เลขอะตอม เพิ่ มขึ้น” และ “ไอออนของ โลหะในคาบ เดียวกันจะมี ขนาดเล็กลง เมือ่ เลขอะตอม เพิ่ มขึ้น” 23 Ionization energy :พลังงานที่ใช้ ในการดึง e- หลุดออกจากในสภาวะก๊ าซ อะตอมใดมีขนาดเล็ก จะทาให้ ดงึ e- ออกยาก อะตอมใดมีขนาดใหญ่ จะทาให้ ดงึ e- ออกง่าย โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน IE สูง IE ต่า 24 ตามคาบ จานวนประจุบวกเพิ่มมากขึ ้น e- อยู่ไกล Nu มาก e- หลุด ง่าย IE ต่า e- หลุดยาก IE สูง First Ionization Energy เพิ่มขึ้น First Ionization Energy เพิม่ ขึ้น ตามหมู่ ระดับ พลังงาน มากขึ ้น e- ถูกดึงดูดมาอยู่ใกล้ Nu ได้ มาก โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 25 Electron Affinity Electron affinity (EA) คือพลังงานที่ปลดปล่อยออกมาจากการรับอิเล็กตรอน ของอะตอมธาตุแล้วเกิดเป็ นแอนไอออน ณ สถานะแก๊ส X (g) + e- X-(g) F (g) + e- F-(g) O (g) + e- O-(g) โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน ธาตุที่มี EA สูง จะคายพลังงานออกมามากเมื่ อรับ อิ เ ล็ก ตรอนเข้ า ไป ท าให้ เ กิ ด ไอออนลบที่ มี ค วาม เสถี ย รมาก ดั ง นั น้ ค่ า EA จึ ง ใช้ ท านาย ความสามารถในการเป็ นไอออนลบ กล่าวคือ ธาตุที่ มี EA สูง จะสามารถเกิดเป็ นไอออนลบได้ ง่ายกว่า ธาตุที่มี EA ต่า 26 Electron Affinity ธาตุใ นหมู่ เ ดี ย วกัน ค่ า EA ลดลงจากบนลงล่าง เพราะ ธาตุข้ า งบนมี ข นาดเล็ ก กว่ า ธาตุข้า งล่า ง จึง มี แ รงดึ ง ดูด ระหว่างประจุบวกที่นิวเคลียส กั บ อิ เ ล็ ก ตรอนที่ เ พิ่ ม เข้ าใน อะตอมได้ มากกว่า ระยะทาง จากนิวเคลียสถึงขอบเขตของ อะตอมสั น้ กว่ า อะตอมที่ มี ขนาดใหญ่ ที่อ ยู่ข้า งล่ างของ ห มู่ ธ า ตุ ข้ า ง บ น รั บ อิ เ ล็ ก ตร อ น ได้ ดี ก ว่ า ธ า ตุ ข้ างล่าง EA จึงมากกว่า ธาตุในคาบเดียวกัน ค่า EA เพิ่มขึ ้นจากซ้ ายไปขวาของตารางธาตุ เพราะธาตุทางขวามีขนาดเล็กกว่าธาตุทางซ้ าย จึงรับ e- ได้ ดกี ว่า e- ที่เข้ ามาใหม่จะถูกดึงดูดด้ วย Nucleus ได้ มากกว่า EA จึงมากกว่า โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 27 Electronegativity อิเล็กโตรเนกาติวิตี ้ ( Electronegativity ) เป็ นค่าสมมติที่แสดงความสามารถในการ ดึงดูดอิเล็กตรอนคูร่ ่วมพันธะจาก Nucleus e- คูร่ ่วมพันธะของอะตอมที่มีขนาดเล็ก จะได้ รับแรงดึงดูดจาก Nucleus มาก EN สูง e- คูร่ ่วมพันธะของอะตอมที่มีขนาดใหญ่ จะได้ รับแรงดึงดูดจาก Nucleus น้ อย EN ต่า อะตอมที่มีสภาพไฟฟ้าลบมาก จะดึงอิเล็กตรอนที่ใช้ ร่วมกันในการเกิด พันธะโคเว เลนต์เข้ าหาตัวเองได้ มากกว่า ได้ มีผ้ หู าค่าสภาพไฟฟ้าลบไว้ หลายแบบ แต่ ที่นิยมใช้ อ้ างอิงมากที่สดุ คือ ของพอลิง โดยกาหนดให้ ฟลูออรี นมีค่าสภาพไฟฟ้าลบมากที่สดุ คือ เท่ากับ 4.0 และซีเซียม ( Cs ) มีสภาพไฟฟ้าลบน้ อยที่สดุ คือเท่ากับ 0.7 โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 28 Electronegativity ธาตุในคาบเดียวกัน ค่า EN จะเพิ่มขึ ้นจากซ้ ายไปขวา เพราะขนาดอะตอมเล็กลงทาให้ ได้ รับแรงดึงดูดจากนิวเคลียสมากกว่าอะตอมที่มีขนาดใหญ่ EN จึงสูงขึ ้น ธาตุหมู่เดี ยวกัน ค่า EN จะลดลงจากบนลงล่ า ง เพราะขนาดอะตอมใหญ่ ขึ น้ ท า ใ ห้ นิ ว เ ค ลี ย ส มี โอกาสดึงดูดอิเล็กตรอน ได้ น้ อยกว่ า อะตอมที่ มี ขนาดเล็ก EN จึงต่าลง โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 29 จุดหลอมเหลวและจุดเดือด ก. โลหะในหมู่เดียวกัน คือ หมู่ IA , IIA, และ IIIA “จุดหลอมเหลวและจุดเดือดมี แนวโน้ มลดลง เมื่อเลขอะตอมเพิ่มขึ ้น” เนื่องจากความแข็งแรงของพันธะโลหะลดลง เพราะมีขนาด อะตอมใหญ่ขึ ้น ข. โลหะในคาบเดียวกัน คือ โลหะในหมู่ IA , IIA, และ IIIA ในคาบต่างๆ “จุดหลอมเหลว และจุดเดือดมีแนวโน้ มสูงขึ ้น เมื่อเลขอะตอมเพิ่มขึ ้น” เนื่องจากมีพนั ธะโลหะที่แข็งแรงมากขึ ้น ทังนี ้ ้ เพราะอะตอมมีขนาดเล็กลงและมีจานวนเวเลนต์อิเล็กตรอนเพิ่มขึ ้น หมายเหตุ สาหรับธาตุหมู่ IVA และ VA จุดหลอมเหลวและจุดเดือดมีแนวโน้ มของการ เปลี่ยนแปลงไม่ชดั เจน เนื่องจากมีโครงสร้ าง และแรงยึดเหนี่ยวระหว่างอะตอมที่แตกต่าง กัน โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน หมู่ IA หมูI่ VA สูง (โลหะ) ต่า 30 จุดหลอมเหลวและจุดเดือด ก.อโลหะในหมู่เดียวกัน คือ หมู่ VIA , VIIA, และ VIIIA “จุดหลอมเหลวและจุดเดือดมีแนวโน้ ม เพิ่มขึ ้น เมื่อเลขอะตอมเพิ่มขึ ้น” เนื่องจากแรงยึดเหนี่ยวระหว่างโมเลกุลคือแรงวันเดอร์ วาลส์เพิ่มขึ ้น เพราะมวลโมเลกุลและขนาดโมเลกุลเพิ่มขึ ้น ข. อโลหะในคาบเดียวกัน คือ อโลหะ หมู่ VA, VIA , VIIA, และ VIIIA “จุดหลอมเหลวและจุดเดือด มีแนวโน้ มลดต่าลงเมื่อเลขอะตอมเพิ่มขึ ้น” เนื่องจาก แรงยึดเหนี่ยวระหว่างโมเลกุลคือ แรงวันเดอร์ วาลส์มี ค่าลดลง เพราะขนาดของโมเลกุลเล็กลง โดยเฉพาะ ก๊ าซเฉื่อยเป็ นก๊ าซประเภทโมเลกุลเดี่ยว และมีขนาด เล็ก มีจดุ หลอมเหลวและจุดเดือดต่ามาก โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน หมู่ VA หมูV่ IIIA ต่า (อโลหะ) สูง 31 Trends in Size, IE, EA and EN Size Ionization energy Electron Affinity Electronegativity โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน Larger Larger Larger Larger Larger Larger Larger Larger 32 แนวโน้ มของสมบัตติ ามตารางธาตุ แนวโน้ มของสมบัตทิ างเคมี 1. เลขออกซิเดชัน 2. ศักย์ รีดักชันมาตรฐาน (E๐) 3. การเข้ าทาปฏิกิริยา โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 33 Oxidation Number เลขออกซิเดชัน ( Oxidation Number ) เป็ นตัวเลขเพื่อแสดงค่าประจุไฟฟ้าหรื อประจุไฟฟ้า สมมติของไอออนหรื ออะตอมของธาตุ ซึง่ ส่วนใหญ่เป็ นเลขจานวนเต็มรวมทังศู ้ นย์และอาจ มีเครื่ องหมายเป็ นบวกหรื อลบก็ได้ การกาหนดค่าเลขออกซิเดชัน มีกฎดังนี ้ คือ 1. อะตอมของธาตุตา่ ง ๆ ในสภาวะอิสระ ไม่วา่ จะอยูใ่ นรูปที่เป็ นอะตอมเดียว หรื อ โมเลกุล จะมีเลขออกซิเดชันเท่ากับศูนย์ เช่น Na Be He O2 S8 2. ไอออนที่มีอะตอมเดี่ยวเลขออกซิเดชันจะมีคา่ เท่ากับประจุของไอออนนัน้ เช่น Na+ มีเลขออกซิเดชัน เท่ากับ +1 Be2+ มีเลขออกซิเดชัน เท่ากับ +2 O2- มีเลขออกซิเดชัน เท่ากับ -2 3. เลขออกซิเดชันของโลหะอัลคาไล ( หมู่ IA ) และโลหะอัลคาไลน์เอิร์ท ( หมู่ IIA ) ในสารประกอบต่าง ๆ มีคา่ เท่ากับ +1 และ +2 ตามลาดับ 34 โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน Oxidation Number 4. เลขออกซิเดชันของออกซิเจนในสารประกอบส่วนมาก มีคา่ เท่ากับ -2 ยกเว้ น •สารประกอบเปอร์ ออกไซด์ เช่น H2O2 และ Na2O2 ออกซิเจนมีเลขออกซิเดชัน -1 •สารประกอบซุปเปอร์ ออกไซด์ เช่น KO2 ออกซิเจนมีเลขออกซิเดชัน -1/2 •สารประกอบ OF2 ออกซิเจนมีเลขออกซิเดชัน +2 5. เลขออกซิเดชันของไฮโดรเจนในสารประกอบส่วนมากมีคา่ เท่ากับ +1 ยกเว้ นใน สารประกอบพวกไฮไดรด์ไอออนิก ซึง่ ไฮโดรเจนมีคา่ เลขออกซิเดชันเท่ากับ -1 เช่น LiAlH4 และ NaBH4 6. ผลรวมทางพีชคณิตของเลขออกซิเดชันของอะตอมทังหมดในสู ้ ตรเคมีใด ๆ จะมีคา่ เท่ากับประจุสาหรับกลุม่ ของอะตอมที่เขียนแสดงในสูตรนัน้ ๆ เช่น ผลรวมของเลข ออกซิเดชันของ KMnO4 เท่ากับ 0 ผลรวมของเลขออกซิเดชันของ NO3- เท่ากับ -1 โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 35 Oxidation Number ตัวอย่างที่1 จงหาเลขออกซิเดชันของ S ใน H2SO4 สมมติเลขออกซิเดชันของ S = x ตัวอย่างที่2 จงหาเลขออกซิเดชันของ Co ใน [Co(CN)6]4- เลขออกซิเดชันของ H = +1 สมมติเลขออกซิเดชันของ Co = x 2 อะตอมของ H มีเลขออกซิเดชันรวม = (+1 2) = +2 เลขออกซิเดชันของ CN- = -1 เลขออกซิเดชันของ O = -2 ผลรวมเลขออกซิเดชันของ CN = (-1 6) = -6 4 อะตอมของ O มีเลขออกซิเดชันรวม = (-2 4) = -8 ผลรวมเลขออกซิเดชันธาตุทงหมดในไอออนเท่ ั้ ากับ ประจุของไอออน ผลรวมของเลขออกซิเดชันธาตุทงหมดในสารประกอบ ั้ เท่ากับ 0 ดังนัน้ +2 + x + (-8) = 0 x = +6 เลขออกซิเดชันของ S ใน H2SO4 = +6 โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน เท่ากับ -4 ดังนัน้ x + (-6) = -4 x = +2 เลขออกซิเดชันของ Co ใน [Co(CN)6]4- = +2 36 Oxidation Number โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 37 ศักย์รีดกั ชันมาตรฐาน (E๐) Li+ + e- Li Li Cs+ + e- Cs Cs เป็ นบวกมากขึ ้น F F2 + 2e- 2F- I I2 + 2e- 2I- ด้ านซ้ าย เป็ นตัวรี ดิวซ์ที่ดีมาก เสียอิเล็กตรอนได้ ง่าย ด้ านขวา โลหะเป็ นตัวรี ดิวซ์ที่เลวลง อโลหะจะเป็ นตัวออกซิไดส์ คือรับอิเล็กตรอน กึ่งโลหะ เฉื่อยต่อการเกิดปฏิกิริยา เนื่องจากมาโครงสร้ างแบบร่ างตาข่ายที่มี ความแข็งแรง โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 38 การเข้าทาปฏิกิริยา 6Li + N2 2Li3N 3Be + N2 Be3N2 2Al + N2 2AlN Sn + N2 ไม่เกิดปฏิกิริยา Sn + O2 SnO2 อุณหภูมิห้อง เผาจนร้ อนแดง เมื่อให้ ความร้ อน เมื่อให้ ความร้ อน Li F โลหะ ว่ องไวมาก Cs โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน ว่ องไวมาก อโลหะ I 40 แนวโน้ มของสมบัตติ ามตารางธาตุ แนวโน้ มความเป็ นกรด-เบสของสารประกอบ 1. ออกไซด์ และไฮดรอกไซด์ 2. ไฮไดรด์ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 41 • ออกไซด์ และไฮดรอกไซด์ – ออกไซด์เป็ นสารประกอบระหว่างธาตุกบั ออกซิเจน Na2O, B2O3, P2O5 – ไฮดรอกไซด์เป็ นสารประกอบที่มีหมู่ –OH เช่น NaOH เป็ นโคเวเลนต์มากขึ ้น IA/1 เป็ นไอออนิก มากขึ ้น เป็ นกรดมากขึ ้น VIIA/17 โคเวเลนต์ ไอออนิก ก ้ากึ่งระหว่างไอออนิก และโคเวเลนต์ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน IA/1 เป็ นเบส มากขึ ้น VIIA/17 โคเวเลนต์ ไอออนิก แอมโฟเทอริ ก 42 • สารประกอบออกไซด์ของธาตุทางซ้ ายมือในตารางธาตุ เป็ นเบสเนื่องจาก เมื่อละลายในน ้า จะได้ สารประกอบไฮดรอกไซด์ ซึง่ สามารถแตกตัวให้ หมู่ ไฮดรอกไซด์ เช่น CaO + H2O Ca(OH)2 Ca2+ + 2OH• สารประกอบออกไซด์ของธาตุทางขวามือในตารางธาตุ เป็ นกรดเนื่องจาก เมื่อละลายในน ้า จะได้ สารประกอบ ซึง่ สามารถแตกตัวให้ H+ ดังนี ้ SiO2 + H2O H2SiO3 SiO32+ + 2H+ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 43 Na2O NaOH MgO Al2O2 Mg(OH)2 Al(OH)3 เบสแก่ เบสอ่ อน SiO2 P2O5 SO3 SiO2.xH2O H3PO4 H2SO4 กรดอ่ อน/เบสอ่ อน กรดอ่ อน HOCl < HClO2 < กรดแก่ ขึน้ HClO3 Cl2O7 HClO4 กรดแก่ < HClO4 H2SO3 < H2SO4 * สารประกอบที่มีออกซิเจนเป็ นองค์ประกอบอยูม่ าก จะมีความเป็ นกรดสูง เนื่องจาก ออกซิเจนมีคา่ EN สูง สามารถดึงอิเล็กตรอนได้ ดี ทาให้ พนั ธะระหว่าง H-O อ่อนลง H+ จึงถูกปลดปล่อยออกได้ ง่าย โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 44 • ความเสถียรของสารประกอบไฮดรอกไซด์ ของโลหะและการละลาย โลหะไอออนที่มีขนาดเล็ก ประจุสงู จะเกิดสารประกอบไฮดรอกไซด์ที่เสถียร เช่น Al3+, Fe3+, Cr3+ เป็ นต้ น ((OH- มีขนาดเล็ก ชอบจับกับแคตไอออนที่มีขนาด เล็ก) ดังนัน้ Al(OH)3 จะเสถียรกว่า Mg(OH)2 เนื่องจาก Al3+ มีขนาดเล็กกว่า และประจุสงู กว่า Mg2+ทาให้ Al(OH)3 ละลายได้ ยากกว่า ในหมูเ่ ดียวกันความเสถียรลดลง จากบนลงล่าง นัน่ คือการละลายมากขึ ้น เมื่อไอออน โลหะมีขนาดใหญ่ขึ ้น ดังค่า Ksp ที่สงู ขึ ้น Be(OH)2 1.6 × 10-26 Mg(OH)2 8.9 × 10-12 Ca(OH)2 1.3 × 10-6 โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 45 • ความเสถียรของสารประกอบซัลเฟตของโลหะและการละลาย แนวโน้ มจะตรงกันข้ ามกับสารประกอบไฮดรอกไซด์ นัน่ คือ ความเสถียรมากขึ ้น การละลายลดลง เมื่อโลหะไอออนมีขนาดใหญ่ขึ ้น (SO42- มีขนาดใหญ่ ชอบจับกับแคตไอออนขนาดใหญ่) CaSO4 2.4 × 10-4 SrSO4 7.6 × 10-7 BaSO4 1.5 × 10-9 สารประกอบ C2O42- และ CrO42- ก็ทานองเดียวกันกับสารประกอบซัลเฟต สรุ ปว่ า size difference น้ อย จะเสถียร โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 46 • สารประกอบไฮไดรด์ • สารประกอบระหว่างธาตุ (M) กับไฮโดรเจน (H) 1. ไฮไดรด์ไอออนิก มีพนั ธะไอออนิกระหว่าง M+ กับ H- ได้ แก่ไฮไดรด์ ของธาตุกลุม่ s เกือบทังหมด ้ 2. ไฮไดรด์เมตาลิก มีอะตอมไฮโดรเจนแทรกอยูใ่ นผลึกโลหะ (interstitial hydride) ได้ แก่ ไฮไดรด์ของธาตุแทรนซิชนั 3. ไฮไดรด์โคเวเลนต์ มีพนั ธะโคเวเลนต์ระหว่างธาตุ M กับไฮโดรเจน (+1) ได้ แก่ไฮไดรด์ของธาตุกลุม่ p เกือบทังหมด ้ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 47 • แนวโน้ มความเป็ นกรด-เบส ของสารประกอบไฮไดรด์ s เบสแก่ p กรดแก่ แนวโน้ มความเป็ นกรด-เบสของไฮไดรด์ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน • ค่า EN ของ M ยิ่งสูงมาก โอกาสที่ H จะ กลายเป็ น H+ เกิดได้ ง่ายขึ ้น • ความแข็งแรงของพันธะ M-H จะเปลี่ยน ตามขนาดของ M ถ้ า M มีขนาดใหญ่ขึ ้น พันธะจะยิ่งอ่อนลง • พันธะไฮโดรเจนระหว่างโมเลกุลของไฮโดรด์ ยิ่งมีมาก โอกาสที่ H จะหลุดไปเป็ น H+ ก็ ยิ่งน้ อยลง 48 ในคาบเดียวกัน • ธาตุ M ที่มีคา่ EN สูง จะดึงอิเล็กตรอนเข้ าหาตัวเองได้ ดี ทาให้ H หลุดไปเป็ น H+ ได้ ง่าย จึงมีความเป็ นกรดสูง NH3 < H2O < HF ในหมู่เดียวกัน • ธาตุ M ที่มีขนาดใหญ่ อิเล็กตรอนวงนอกซึง่ สร้ างพันธะกับ H อยู่ ไกลกับนิวเคลียสมาก พันธะ M-H จะอ่อนลง ทาให้ H หลุดไป เป็ น H+ ได้ ง่าย จึงมีความเป็ นกรดสูง HF < HCl < HBr < HI โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 49 Main Group Hydrogen is the simplest element in the Periodic Table Hydrogen has, in simplistic terms, three different ways in which it forms chemical compounds: lose its single electron to form a proton: H+ share an electron through formation of covalent bonds gain an electron, to form the hydride ion: H- โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 50 Occurrence and Manufacture Hydrogen is the most abundant element in the universe, followed by helium. H2 can be prepared by several methods: 1) Electrolysis Or 2) Reforming of hydrocarbons 3) Hydrolysis of an ionic hydride โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 51 Occurrence and Manufacture Group 1 metals, calcium, strontium and barium react with water 2Na + 2H2O 2NaOH + H2 Less reactive metals such as Mg Zn and Tn dissolved in acids such as HCl: Mg + 2HCl MgCl2 + H2 4 g of hydrogen is 2 moles, so 484 kJ of energy would be produced. Hydrogen is an energy-rich fuel, and combustion product is simply water So hydrogen is a very attractive fuel and is increasingly being used in transportation systems worldwide. โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 52 Isotopes of Hydrogen Tritium is formed by cosmic ray bombardment of 14N in the upper atmosphere, or in a nuclear reactor, where Li is bombarded with neutrons (n) โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 53 Hydrides Hydride react with water: Group 13 B2H6 (AlH3)n 14 CnH2n+2 CnH2n CnH2n-2 etc. SinH2n+2 (n8) 15 NH3 N2H4 16 H2O H2O2 17 HF PH3 H2S HCl GenH2n+2 (n9) P2H4 AsH3 H2Sn H2Se HBr SnH4 SbH3 H2Te HI โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 54 Reaction 1) Direct combination 2) Reduction of halide 3) Hydrolysis 4) Interconversion of hydride โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 55 a) Na2S + HCl H2S + 2NaCl b) 2PhPCl2 + LiAlH4 2PhPH2 + LiAlCl4 โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 56 The Group 1 (Alkali Metal) Lithium, Sodium, Potassium, Rubidium, Caesium and Francium The chemistry of the alkali metals is dominated by the tendency to lose the single s-electron and attain a noble gas electronic configuration 600 First ionization energies 500 Have e- in d-orbital kJ/mol 400 300 200 Low shielding 100 0 Li Na โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน K Rb Cs 57 Slater’s rule The rules for determining S for a specific electron are as follows: The electronic structure of the atom is written in groupings as follows: (1s) (2s,2p) (3s,3p) (3d) (4s,4p) (4d) (4f) (5s,5p), etc. Electrons in higher groups (to the right in the list above) do not shield those in lower groups. For ns or np valence electrons: • Electrons in the same ns, np group contribute 0.35, except the 1s, where 0.30 works better. • Electrons in the n - 1 shell contribute 0.85. • Electrons in the n - 2 or lower contribute 1.00. For nd and nf valence electrons: • Electrons in the same nd or nf group contribute 0.35. • Electrons in groups to the left contribute 1.00. โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 58 Physical properties โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 59 E0 of group 1 M(s) M+(aq) + e- Hnet = Hsub + IE + Hhyd Hnet คือ เอนทาลปีสทุ ธิ Hsub คือ พลังงานการระเหิด IE คือ พลังงานไอออไนเซชัน Hhyd คือ พลังงานไฮเดรชัน โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 60 Alkali metal crystalline The alkali metals crystallize in body-centred cubic lattices Blue โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 61 Reaction The metals react with water, lithium relatively slowly, but with increasing vigor going down the group The hydroxides absorb CO2 to give the alkali metal carbonate M2CO3 or the hydrogencarbonate (bicarbonate) MHCO3. The hydrogencarbonates decompose on heating to give the carbonates, which themselves decompose on stronger heating to give the oxide plus carbon dioxide The nitrates MNO3 (M = Na, K, Rb, Cs) decompose to the nitrites on heating while, in contrast, LiNO3 decomposes to Li2O (+ NO2 + O2). โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 62 Alkali metal halides 0.732 – 1.00 CsCl a) CsCl โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 0.414 – 0.732 NaCl b) NaCl 63 Reaction Compound with nitrogen: Only Li react with nitrogen N3- Lithium azide Compound with phosphorus: include P As Sb โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 64 Reaction Compound with Oxygen and Sulfur โลหะ Li Na K, Rb, Cs Li2O โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน ผลิตภัณฑ์ทข่ี น้ึ Li2O Na2O2 MO2 Na2O2 Anion ของผลิตภัณฑ์ทเ่ี กิดขึน้ O2- (oxide) O22- (peroxide) O2- (superoxide) MO2 65 Reaction Compound with halogen Compound with hydrogen Alkali metal complex โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 66 Diagonal relation โดยทัวไป ่ ธาตุหมูเ่ ดียวกันจะมีสมบัตคิ ล้ายกัน แต่พบว่า Li มีสมบัตคิ ล้ายคลึงกับ Mg ทีอ่ ยูใ่ นธาตุหมู่ 2 เช่น Li กับ Mg ทาปฏิกริ ยิ ากับ N2 ทีอ่ ุณหภูมสิ งู ได้โลหะไนไตรด์แต่ โลหะตัวอื่นไม่ทา โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 67 Group2: Alkali earth metals The Group 2 Elements: Beryllium, Magnesium, Calcium, Strontium, Barium and Radium Relative abundances in the Earth’s crust of the alkaline earth metals โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 68 Physical properties Some physical properties of the alkaline earth metals, M, and their ions, M2+ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 69 Ca2+ Ca+ and Ca3+ หากพิจารณาพลังงานไอออไนเซชันที่ 1, 2 และ 3 พบว่า เหตุใดหมู่ 2 จึงไม่มีเลขออกซิเดชัน +1 แต่จะพบเลข ออกซิเดชัน +2 ค่าเดียว เหตุผลเนื่องจาก พลังงานไฮเดร ชันมีผลต่อความเสถียรของไอออน และพลังงานไฮเดรชัน ขึ ้นกับศักย์ไอออนิก ดังนั ้นไอออน +2 มีขนาดเล็กกว่า ไอออน +1 ย่อมมีพลังงานไฮเดรชันสูงกว่า เมื่อพิจารณา แผนภาพพลังงานพบว่า ถึงแม้ ว่าการเกิดเป็ น Ca2+(g) จะ ใช้ พลังงานมากกว่าการเกิด Ca+(g) แต่พลังงานไฮเดรชัน ของ Ca2+ ที่มากกว่า Ca+ ทาให้ Ca2+(aq) มีพลังงาน ที่ต่ากว่า Ca+(aq) และสถานะของแข็ง Ca2+ มีพลังงาน แลตติซสูงกว่า Ca+ เนื่องจากมีประจุมากกว่าและขนาด ไอออนเล็กกว่า ดังนั ้นผลึกไอออนิก Ca2+ จึงเสถียรกว่า Ca+ ทาให้ โลหะหมู่ 2 มีเลขออกซิเดชัน +2 ส่วน Ca3+ ไม่ เกิดเพราะพลังงานในการเกิดไอออน +3 สูงมาก โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 70 Solubility Be2+ Mg2+ Ca2+ Sr2+ Ba2+ SO42- CO32- C2O42- CrO42- OH- F- 2.4x10-4 7.6x10-7 1.5x10-9 1.0x10-5 4.7x10-9 7.0x10-10 1.6x10-9 8.6x10-5 1.3x10-9 5.6x10-8 1.5x10-12 7.1x10-4 3.6x10-5 8.5x10-11 1.6x10-26 8.9x10-12 1.3x10-6 3.2x10-4 5.0x10-3 8.0x10-8 1.7x10-10 7.9x10-10 2.4x10-5 การละลาย พลังงานแลตติซ (r+ กับ r- ) และพลังงานไฮเดรชัน (ขนาดของแต่ละไอออน) สารประกอบ ซัลเฟต คาร์ บอเนต ออกซาเลต และโครเมต ขึ ้นกับ พลังงานไฮเดรชัน สารประกอบ ไฮดรอกไซด์ และฟลูออไรด์ ขึ ้นกับ พลังงานแลตติซ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 71 • หากพิจารณาสมบัติการละลายซึง่ เราสามารถพิจารณาได้ จากพลังงานแลตติซซึง่ ขึ ้นกับ ระยะห่างระหว่าง r+ กับ r- และพลังงานไฮเดรชันขึ ้นกับขนาดของแต่ละไอออนในสารประกอบ ไอออนิก ผลการละลายพบว่า • 1) สารประกอบ ซัลเฟต คาร์ บอเนต ออกซาเลต และโครเมต ขนาดไอออนของโลหะ ใหญ่ขึ ้น การละลายน้ อยลง ไอออนลบมีขนาดใหญ่ การเพิ่มไอออนบวกจะไม่มีผลให้ r++rเปลี่ยนแปลงน้ อย พลังงานแลตติซจึงเกือบคงที่ แต่พลังงานไฮเดรชันจะลดลง ประจุต่อ ขนาดอะตอมน้ อยลงการละลายน้ อยลง • 2) สารประกอบ ไฮดรอกไซด์ และฟลูออไรด์ ขนาดไอออนของโลหะใหญ่ขึ ้นการละลาย เพิ่มขึ ้น ไอออนลบมีขนาดเล็ก ดังนันท ้ าให้ r++r- เพิ่ม พลังงานแลตติซจึงลดลง (พลังงาน แลตติซแปลผกผันกับ (r++ r-) โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 72 Compound Group 2 simple anhydrous compounds of beryllium tend to be covalent in nature [Be( H2O)4]2+ therefore only exists in strong acid solutions โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 73 Compound Group 2 Ans: The major difference between beryllium and aluminium is due to absolute size: aluminum, being larger, froms six-coordidate [Al(H2O)6]3+ while beryllium forms four-coordinate [Be(H2O)4]2+ โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 74 MX2 gas > The structures of gaseous group 2 metal fluoride and later halide molecules are summarized in Table and are the subject of ongoing theoretical interest. The term ‘quasilinear’ refers to a species for which the calculated energy difference between linear and bent structures > Two main point describe the shape of molecule that is polarization and and orbital. > Be and Mg form only linear gaseous dihalides. These two metals have only s and p atomic orbitals For Ca, Sr and Ba, vacant 3d, 4d and 5d orbitals, respectively, are available, but can only overlap efficiently with orbitals on the X atoms if the MX2 molecule is bent โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 75 Solid state The structure is based on a facecentred cubic lattice of Ca2+ ions, with F- ions in all of the tetrahedral holes โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 76 Reaction of Group 2 Reaction with water Be does not react with water Hot water Ca Sr และ Ba ทาปฏิกิริยาที่อณ ุ หภูมิห้อง โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 77 Reaction of Group 2 When heated, all the group 2 metals combine with O2, N2, sulfur or halogens the nitrides react with water to produce ammonia โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 78 Hydrides All of the Group 2 metals except beryllium form an ionic dihydride, MH2, on heating the metal in hydrogen. BeH2, which is stable, must be synthesized indirectly by pyrolysis of di-tert-butylberyllium โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 79 Q: propose mechanism of BeH2 from pyrolysis of di-tertbutylberyllium BeH2 ที่เป็ นของแข็งเกิด Be-H-Be bridges เกิดพันธะที่เรี ยกว่ า tree-centretwo-electron bonds ซึ่งการเกิด bridge ดังกล่ าวเหมือนกับการเกิด diborane (B2H6) โรงเรียนมหิดลวิทยานุสรณ์ องค์การมหาชน 80