南台科技大學 生物科技系 學生專題 擴展核多角體病毒寄主範圍之研究
advertisement

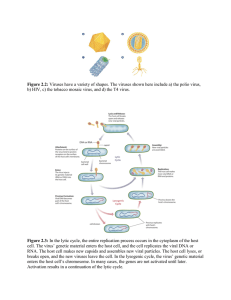
南台科技大學 生物科技系 學生專題 擴展核多角體病毒寄主範圍之研究 學生:495H0002 蕭宇璇 指導教授:李松泰 中華民國九十九年五月 1 摘要 本實驗室初步研究發現加州苜蓿夜蛾核多角體病毒台灣本土分離株 AcMNPV-TW4 比外國分離的病毒株 AcMNPV-E2 及 AcMNPV-C6 對昆蟲細胞及小菜蛾昆蟲具有更高的感 染效率。本研究主要是以蛋白質體學的方法ㄧ維電泳的技術,來探討 AcMNPV-TW4 與 國外分離的 AcMNPV-E2 及 AcMNPV-C6 的差異。結果顯示 AcMNPV-TW4 與 AcMNPV-C6 的 圖譜非常相似,而與 AcMNPV-E2 封埋體的蛋白質圖譜,具有極大的差異。 2 目 次 摘要 2 目次 3 第一章 前言 4 第二章 文獻探討 5 2.1 昆蟲桿狀病毒之構造 5 2.2 昆蟲桿狀病毒生活史 5 2.3 昆蟲桿狀病毒之分類 6 第三章 材料及方法 9 3.1 昆蟲細胞與培養 9 3.2 狀病的來源與配置 9 3.3 SDS-PAGE 10 3.4 Coomassie blue 染色 10 第四章 結果與討論 11 參考文獻 14 3 第一章 前言 生物農藥是以大自然之生物、微生物或其天然產物為資材,經由生物程序製造、 具有專一性及安全性(無毒性)之植物保護製劑。因為生物農藥不會對大自然生態環 境造成不良的衝擊、安全性高,無化學農藥之缺點,所以生物農藥的發展已成為時勢 之所趨,日益受到先進國家重視,也是我國農業升級不可或缺的要員。包括核多角體 病毒在內的昆蟲桿狀病毒,是發展生物農藥的重要資材。但是以微生物開發出來的 生物農藥,其特性之ㄧ就是有些微生物本身具有地域性的差異。加州苜蓿夜蛾核多 角體病毒(Autographa californica multiple nucleopolyhedrovirus 簡稱為 AcMNPV), 是目前所知唯一較廣譜性的昆蟲桿狀病毒,它可以感染包括小菜蛾、甜菜夜蛾及擬 尺蠖等至少二十多種鱗翅目昆蟲。從自然界分離的 AcMNPV 對昆蟲的感染能力, 可能因為不同地區而有差異。1992 年 David R.O’Reilly 等人所發表的文獻中指出, 不同種類的桿狀病毒會具有極大的差異性,但即使同種類但不同分離株的病毒也同樣 有可能具有差異,但目前有關不同 AcMNPV 病毒分離株之特性比較的研究很少。 我們實驗室獲得一株台灣本土分離的 AcMNPV 病毒株命名為 AcMNPV-TW4,初 步與國外分離的病毒株 AcMNPV-E2 及 AcMNPV-C6 比較對昆蟲細胞及小菜蛾昆蟲的 感染效率,發現 AcMNPV-TW4 感染效率最高,其次是 AcMNPV-C6,AcMNPV-E2 效果最差。因此 AcMNPV-TW4 除了具有開發成生物農藥的潛能外,亦是探討不同病 毒株感染昆蟲時致病機制差異性的良好題材。因為在自然環境中,昆蟲因食入桿狀病 毒之封埋體而開始受感染。因此本研究將比較本土分離的這株 AcMNPV-TW4,與另 外二株國外分離的病毒株 AcMNPV-E2 及 AcMNPV-C6,封埋體蛋白質圖譜之差異性。 我們將以 AcMNPV 病毒的宿主細胞 Sf-9 來大量製備這三株病毒,之後將其封埋體分 離出來,以 SDS-PAGE 來比較這三株病毒封埋體的差異性。若能找出有差異的蛋白 質,再進一步針對這些蛋白質送去鑑定,及探討它們的功能。 4 第二章 文獻探討 2.1 昆蟲桿狀病毒之構造 桿狀病毒是具有被膜(envelope) 的雙股 DNA 病毒(Burgess, 1977)。它的核蛋白 鞘(nucleocapsid)是由鞘蛋白(capsid protein)所形成的蛋白質外鞘(capsid) ,及裡 面由 DNA 與蛋白質所形成的核心組成。此 DNA 與蛋白質核心,含有一個 80~180kb 之環狀雙股 DNA 基因體及某些蛋白質。核蛋白鞘呈桿狀,大小為 30-60 X 250-300nm (Harrap, 1972;Summers and Anderson, 1972; Tweeten et al., 1980)。在核蛋白鞘外再 覆以被膜而成為病毒粒子(virus particles or virions) 。但有二種不同形態的病毒粒子, 會在生活史中不同時期產生(Blissard and Rohrmann, 1990)。一種是感染初期以出芽 方式產生的病毒粒子稱為胞外病毒(extracellular virus 簡稱 ECV) ,又稱為 budded virus (BV)或 nonoccluded virus(NOV)。另一種是感染末期留在細胞內被包裹在包含 體(occlusion body 或 inclusion body 又稱為 polyhedron)內的病毒粒子,被稱為封埋 體病毒(Occluded virus 簡稱為 OV)。包含體是由多角體蛋白(polyhedrin)所形成的結 晶構造,具有保護病毒粒子的功能。 2.2 昆蟲桿狀病毒生活史 在自然環境中,昆蟲因食入桿狀病毒之封埋體而受感染。在昆蟲中腸鹼性環境 (pH9.0~11.5)及酵素作用下,包含體被溶解釋出病毒粒子(Harrap and Longworth 1974)。此病毒粒子藉其被膜與昆蟲中腸上皮層細胞(epithelial cells)的微絨毛 (microvilli)膜融合,使核蛋白鞘進入細胞(Granados and Williams, 1986),此為桿 狀病毒生活史中的初級感染(primary infection)。核蛋白鞘進入細胞後釋出病毒基因體 進入細胞核,開始早期基因(early gene)的表現。早期基因的表現是以寄主細胞的 RNA polymerase II 進行轉錄作用,合成病毒複製 DNA 及晚期(late)最晚期(very late) 基因表現時所需的蛋白質。晚期基因在 DNA 複製時開始表現,且利用病毒自己的 RNA polymerase 進行轉錄作用(Hoh and Weaver 1990),其產物主要是病毒的構造蛋白。 5 一般在感染後 8 小時後,即有核蛋白鞘在細胞核內產生。此核蛋白鞘以出芽方式釋出 時,以寄主細胞之細胞膜被覆在病毒粒子外面成為病毒粒子的被膜,此病毒粒子即為 胞外病毒。被覆在胞外病毒粒子的被膜雖然是來自感染細胞的細胞膜,但是上面含有 病毒基因表現製造的病毒蛋白質如 gp64(Volkman et al., 1984) 。胞外病毒的被膜呈疏 鬆狀,且一個被膜內只含一個核蛋白鞘,在病毒粒子的一端具膨大結構稱為 peplomers。胞外病毒由中腸細胞釋出穿過基底層到達血液中,藉由血液循環或經由氣 管 系 統 散 佈 至 蟲 體 各 處 (Keddie et al. 1989,Engelhard et al. 1994) , 以 胞 吞 作 用 (endocytosis)方式感染進入昆蟲其它組織器官細胞如脂肪體、血球、肌肉,造成全 身性感染,此為桿狀病毒生活史中的次級感染(secondary infection)。病毒在各個受感 染細胞內進行基因表現、複製基因體、合成病毒的外鞘蛋白。在感染末期,最晚期基 因即多角體蛋白基因及 P10 基因大量表現時,寄主細胞的基因以及大部分病毒早期基 因的表現都被抑制,此時可以發現到細胞核變大的現象,呈透明狀的構造稱為 virogenic stroma 出現在細胞內。組裝完成的病毒核蛋白鞘大量聚集於細胞核內,並覆 以在核中組成的被膜形成病毒粒子,且包裹於包含體內。因此,這種病毒被稱為封埋 體病毒(occluded virus 簡稱為 OV)。罹病的幼蟲會往上爬行,當身體組織被病毒大 量繁殖後呈液化現象,也造成蟲體死亡(Miller, 1997)。在昆蟲死亡後,包含體病毒能 散佈到環境中,並受到包含體的保護,可忍受不良環境因子如紫外線,乾燥氣候等的 破壞(Kelly, 1982; Bilimoria, 1986; Blizzard and Rohrmann, 1990)。桿狀病毒因為生活 史中產生的病毒粒子具有這兩種不同的型態,所以其生活史被稱為雙相複製生活史 (biphasic replication cycle)。 2.3 昆蟲桿狀病毒之分類 早年桿狀病毒科(Baculoviridae)在分類上只有一個桿狀病毒屬(Baculovirus), 屬下有三個亞屬:第一個亞屬為核多角體病毒(nuclear polyhedrosis virus 簡稱 NPV) 。 第二個亞屬為顆粒體病毒(granulosis virus 簡稱 GV),此兩個亞屬皆能形成包含體。 6 第三個亞屬則是由缺乏多角體蛋白基因,不能形成包含的桿狀病毒成員所組成,稱為 無包含體病毒(nonoccluded virus 稱稱 NOV)(Bilimoria, 1986),然此處所稱的 NOV 與胞外病毒的簡稱 NOV 意義不同。1991 年 Wilson 將桿狀病毒科分為真桿狀病毒亞 科(Eubaculovirinae)及裸桿狀病毒亞科(Nudibaculo- virinae) 。真桿狀病毒亞科包括 能形包含體的核多角體病毒屬及顆粒體病毒屬,裸桿狀病毒亞科只有無包含體桿狀病 毒屬。今日病毒分類已將裸桿狀病毒自桿狀病毒科分離出來,成為一群尚未定位的 病毒(2005)。因此,目前桿狀病毒科是依其包含體的組成與結構之不同,分為兩 個屬:即核多角體病毒 (nucleopolyhedrovirus NPV)和顆粒體病毒 (granulovirus GV)。核多角體病毒依病毒粒子內的核蛋白鞘數目可分為單核多角體病毒(single envelope nuclocapsid NPV,SNPV)與繁核多角體病毒(multiple envelope nuclocapsid NPV,MNPV)。SNPV 在每個病毒粒子的被膜內只包裹一個核蛋白鞘;而 MNPV 在每個病毒粒子的被膜內則包裹著多個核蛋白鞘。核多角體病毒的包含體是由多角 體蛋白(polyhedrin)組成,多角體蛋白大小約為 25~31 kDa,結晶時呈多角型。核多 角體病毒又依據一個細胞內可產生包含體數量的多寡分成眾多角體型 (multiple polyhedra type, 簡稱 M type)及寡多角體型(few polyhedra type, 簡稱 F type)。M type 的核多角體病毒在每個細胞內可產生超過十個以上的包含體;而 F type 的核多角 體病毒在每個細胞內產生的包含體數量都在十個以下。顆粒體病毒在每個細胞內只 產生少數包含體,而每個包含體內通常也只含一個病毒粒子,裡面內只有一個核蛋 白鞘,而且只有在鱗翅目昆蟲有發現(Blizzard and Rohrmann,1990;Winstanley and O’Reilly, 1999)。顆粒體病毒之包含體是由顆粒體蛋白(granulin)所組成,此蛋白的 大小約為 25~30kDa,會形成顆粒狀的包含體結晶。桿狀病毒的包含體有助於病毒 對抗惡劣環境,如紫外線、乾燥及其他化學因子(Wang, 1995),並能持續地維持 感染力。 根據多角體蛋白單一基因序列的分析,可將感染鱗翅目昆蟲的核多角體病毒分成 Group I 與 Group II 兩群(Bulach et al. 1999;Zanotto et al. 1993)。另外,胞外病毒進行 胞吞作用時,病毒粒子被膜上的融合蛋白(fusion protein)扮演重要的功能。若以融合蛋 7 白的型式作為區分依據時,所得結果也與上述的分類情形具有一致性(Pearson and Rohrmann, 2002)。Group I NPVs 的套膜上具有 GP64 融合蛋白,而 Group II NPVs 則 不具有相似 gp64 的基因(Pearson et al. 2002)。最近研究學者比對多種昆蟲桿狀病毒基 因序列,提出演化上桿狀病毒可分成四個主要類群:分別是感染鱗翅目的 NPV、感 染鱗翅目的 GV、感染膜翅目的桿狀病毒及感染雙翅目的桿狀病毒(Okano et al. 2006)。 8 第三章 材料及方法 3.1 昆蟲細胞與培養 SF-9 細胞是一株由秋行軍蟲(Spodoptera frugiperda)卵巢組織建立起來的細胞 株,常被用來作為加州苜蓿核多角體病毒體外培養的宿主細胞。由食品工業發展研 究院購買(菌種編號 CCRC60011 )細胞株,以添加 10%胎牛血清 (FBS) 之 TC-100 培養液培養於 26℃培養箱 (MEMMERT/GERMANY, Model : IPP 400) 中,視細胞 數目大約每 2~3 天繼代一次。 3.2 病毒的來源與製備 本 實 驗 使 用 兩 株 國 外 的 加 州 苜 蓿 夜 蛾 核 多 角 體 病 毒 AcMNPV-E2 及 AcMNPV-C6,由中央研究院分生所 521 實驗室趙裕展老師提供。台灣本土分離的 AcMNPV- TW4,是國立台灣大學王重雄老師由罹病的甜菜夜蛾分離而得 (S. S. Kao et al., 2000)。 出芽病毒的配置是將 SF-9 細胞放大至 75T-flask,待長滿約 8~9 成滿細胞之 75T-flask 去掉舊的培養液後,以 moi=0.05 pfu/cell 的病毒液加入 flask,加入不含胎牛 血清之 TC-100 培養液補至 1ml,並放置於擺動式混合器(YOUNG CHENN, Model : SC-30)上緩慢搖擺,感染至少 2 小時後,加入新鮮的培養液至 10ml,並置於 26℃培 養箱中培養。 將三株病毒感染 7~8 天,可觀察到幾乎所有細胞皆完全被感染且產生封埋體,此時 應有大部分細胞皆以病變死亡,將所有的細胞沖下後,4℃下 5000g 離心 30 分鐘, 小心去掉上清,留下細胞 pellet,然後加入 2ml 1% SDS,並震盪 (vortex) 至細胞 全部溶解後置於 42℃水浴中 2 小時,期間每隔 15 分鐘震盪 30 秒,最後以鏡檢方 式觀察細胞是否全部破裂 (如沒有則再加入更多 1% SDS) ,之後加入 3 倍無菌去 離子水,震盪完全後,4℃下 5000g 離心 30 分鐘,去掉上清,再加入適量無菌去離 子水震盪完全後,重複離心步驟,至少進行 5 次重複,要將 SDS 清洗乾淨。最後 9 以適量無菌去離子水回溶封埋體後,儲存於 4℃冰箱中備用。 3.3 SDS-PAGE(SDS-polyacrylamide gel electrophoresis) 取適量之封埋體病毒 1×108,加入同體積的 2X sample buffer,並充分混勻,之 後置於 100℃乾浴槽中加熱 20 分鐘,並每隔 5 分鐘拿出震盪約 15 秒。 製備好 11cm 之膠片 (此電泳系統為 Hofer) ,並將上述處理好之蛋白質樣品注入至 well 中,之後先以 100 V 電壓跑電泳,當 sample 跑過介面 (stacking gel) 後,調整 電壓至 150V,跑膠時間約為 3.5~4 小時,待藍色指示劑跑至最底部時,便可停止 通電,並將膠片取出後,浸泡於 fixation solution 溶液中浸泡至少 1 小時以固定膠 片中的蛋白質。 3.4 Coomassie blue 染色 將跑完 SDS-PAGE 的膠片以去離子水洗滌 3 次,每次 10 分鐘,再置入適量的 coomassie blue 染劑呈色 30 分鐘至 1 小時,最後掃描膠片於電腦中。 10 第四章 結果與討論 昆蟲在自然環境中,因食入桿狀病毒之封埋體而受感染。病毒封埋體在昆蟲中腸 鹼性環境(pH9.0~11.5)及酵素作用下,封埋體被溶解釋出病毒粒子。此病毒粒子藉 其被膜與昆蟲中腸上皮層細胞(epithelial cells)的微絨毛(microvilli)膜融合,使核 蛋白鞘進入細胞,完成桿狀病毒初級感染(primary infection) 的生活史。因此,封埋體 本身所含的蛋白質可能是影響病毒感染寄主能力的因子之ㄧ。本實驗室前人研究發現 加州苜蓿夜蛾核多角體病毒台灣本土分離株 AcMNPV-TW4,與國外分離的兩株病毒 AcMNPV-E2 及 AcMNPV-C6 感 染 小 菜 蛾 之 致 死 效 果 有 明 顯 的 差 異 。 三 者 AcMNPV-TW4 感染效率最高,其次是 AcMNPV-C6,AcMNPV-E2 效果最差。本研究 目的是希望藉由蛋白質體學ㄧ維電泳的技術,探討台灣本土分離株 AcMNPV-TW4 與 國外分離的 AcMNPV-E2 及 AcMNPV-C6 的差異。希望由這些差異能夠了解,同種 病毒之不同病毒株,為什麼對寄主的致病能會有差異的機制。 製備上述三種加州苜蓿夜蛾核多角體病毒之封埋體蛋白質後,各取 30ug 的蛋白 質進行電泳。比較三者蛋白質圖譜的結果顯示,AcMNPV-TW4 與 AcMNPV-C6 的圖 譜非常相似,而與 AcMNPV-E2 封埋體的蛋白質圖譜具有明顯的差異(圖一)。 AcMNPV-E2 在大約 12.3kDa 和 16.96kDa 的蛋白質,與另兩種病毒株 AcMNPV-TW4 及 AcMNPV-C6 的位置有差異性。 在這整個實驗中我們進行了一些基礎研究,而後我們將蛋白質體學應用在此三株 桿狀病毒的研究上,利用二維電泳蛋白質體學分析,我們可以直接的針對病毒的表現 做最正確的評估,在出芽病毒和封埋體病毒是否都具有差異,而未來我們也可以將繼 續解開在蛋白質電泳結果中所看到的差異片段的蛋白質究竟為何,針對差異也可以利 用 LC/MS-MS 來進行蛋白質的定序,一但解開這些蛋白質的關鍵,便可以回到分生 的層次去做更進一步的研究,而過去對於桿狀病毒的研究總是用單獨的病毒株或是不 同種類的病毒株進行比較,這樣的差異太大不足以完全的可以解開桿狀病毒神秘的面 紗,而利用三株同種但是不同分離株的病毒來進行研究,正好提供了一個非常好的研 11 究平台可以研究桿狀病毒的基因調控,一但可以解開桿狀病毒在生活史中的部分調控 機制,那麼,這些結果我們相信可以提升目前桿狀病毒的整體應用價值,不論是在作 為生物農藥、外源蛋白的生產、或是作為基因治療的工具,這都是非常具有幫助的。 12 M E2 TW4 C6 圖一:三株加州苜蓿夜蛾核多角體病毒之封埋體蛋白質圖譜,由左至右為 Maker、 AcMNPV-E2 、 AcMNPV- TW4 、 AcMNPV-C6 。 由 圖 可 發 現 AcMNPV- TW4 、 AcMNPV-C6 兩者相近,而我們由內插法得知三株病毒株在 12.3kDa 和 16.96kDa 的地方有差異性。 13 參考文獻 1. Ahmed, R. and J. G. Stevens. 1990. Viral persistence, pp. 241-265 "Virology" 2ed. B. N. Field et al. [eds.] Raven Press. Ltd. New York. 2. Booker, R. H. 1963. Notes on the pest complex of cowpea in Northern Nigeria. Proc. 1st. Nigerian Grain Legume Conf., Inst. Agric. Res.,Samare, Zaria, Nigeria, pp.9-12. 3. Burand, J. P., H. A.Wood, , and Summers, M. D. 1983a. Defective particles from a persistent baculovirus infection in Trichoplusia ni tissue culture cells. J. Gen. Virol. 64:391-398. 4. Burand, J. P., B. Stiles, and H. A. Wood. 1983b. Structural and intracellular proteins of the nonoccluded baculovirus Hz-1. J. Virol. 46:137-142. 5. Burand, J. P., and H. A. Wood. 1986. Intracellular protein synthesis during standard and defective Hz-1 virus replication. J. Gen. Virol. 67:167-173. 6. Carson, D. D., M. D. Summers, and L. A. Guarino. 1991. Transient expression of the Autographa californica nuclear polyhedrosis virus immediate-early gene, IE-N, is regulated by three viral elements. J. Virol. 65:945-951. 7. Chao, J.T. , P. W. Schaefer, Y. B. Fan, and S. S.Lu. 1996. Host plants and infestation of casuarinas moth Lymantria xylina(Lepidoptera:Lymantriidae)in Taiwan. Quart. J. Chinese For. 11:23-28.(In Chinese) 8. Chao, Y. C., Sheu, S. S., Chang, M. C., Chang, C. Y., Chen, C. W., Weng, H. C., Lin, Y. C., and Lin, H. D. 1990a. Investigation the nature of viral persistent infections using Hz-1 baculovirus as a model system. Bulletin of the Institute of Zoology, Academia Sinica, Monograph 15:33-47 9. Chao, Y.-C. and H. A.Wood, 1990b. The physical map of Hz-1 viral genome from standard and defective interference viral particles. J. Gen. Virol. 71: 1265-1270. 10. Chao, Y. C., H. A. Wood, C. Y. Chang, H. R. Lee, and H. T Lee. 1992. Differential expression of Hz-1 baculovirus genes during viral productive and persistent infections. J. Virol. 66:1442-1448. 11. Chao, Y. C., S. T. Lee, M. C. Chang, H. H. Chen, S. S. Chen, T. Y. Wu, F. H. Liu, E. L. Hsu, R. F. Hou. 1998. A 2.9-Kilobase noncoding nuclear RNA functions in the establishment of persistent Hz-1 viral infection. J. Virology 72(3):2233-2245. 12. Chen, H. H., S. T. Lee, C. T. Chen, and W. S. Wu. 2000. The use of a modified tetracycline regulatory expression system with reduced basal level to development an in vivo biopesticide expression system. Food Science and Agricultural Chemistry. 2(4)220-225. 13. Chen, H. H., F. Y. Tsai and C. T. Chen. 2001a. Negative regulatory regions of the PAT1 of Hz-1 virus contain GATA elements which associate with celllular factors 14 and regulate promoter activity. J. Gen. Virol. 82:313-320. 14. Chen, H. H., D. J. Tso, W. B. Yeh, H. J. Cheng and T. F. Wu. 2001b. The thymidylate synthase gene of Hz-1 virus: agene captured from its lepidopteran host. Insect Molecular Biol. 10(5):495-503. 15. Cheng, S., Xie, Q., Li, Y., Zhu, Z. 1987. Bioassay on the infectivity and field trials of nuclear polyhedrosis virus virus against Lymantria xylina. Chinese Journal Biological control 3(1):33-34. (In Chinese) 16. Crawford, A. M., and L. K. Miller. 1988. Characterization of an early gene accelerating expression of late genes of the baculovirus Autographa californica nuclear polyhedrosis virus. J. Virol. 62:2773-2781. 17. Evans H. F. 1986. Ecology and epizootiology of baculoviruses. pp. 89-132. "The biology of baculoviruses " vol. 2, Granados, R. R. and B. A. Federici [eds.]. 275pp. CRC Press Inc. Bota Raton, Florida. 18. Friesen, P. D., and L. K. Miller. 1986. The regulation of baculovirus gene expression, pp. 31-50. "The molecular biology of baculovirus" Doerfler, W. and P. Boehm [eds.] Springer-Verlag, Berlin. 19. Granados, R. R., Nguyen, T., and Cato, B. 1978. An insect cell line persistently infected with a baculovirus-like particle. Intervirol. 10:309-317. 20. Guarino, L. A., and M. D. Summers. 1987. Nucleotide sequence and temporal expression of a baculovirus regulatory gene. J. Virol. 61: 2091-2099. 21. Guarino, L. A., and M. D. Summers. 1986. Functional mapping of a trans-activating gene required for expression of a baculovirus delayed-early gene. J. Virol. 57:563-571. 22. Hink,W. F. 1972. Insect tissue culture. Adv. Appl. Microbiol. 15:157 23. Hu, R., Ma, Y., Xu, J. Meng, X. 2002. Virulence of AcNPV·Bt·En Formulation Against Spodoptera exigua Larvae. Chinese Journal Biological control 18(1): 47-49.(In Chinese) 24. Huang, Y. Hedberg, J. and Kawanishi, C. Y. 1982. Characterization of the DNA of a nonoccluded baculovirus, Hz-1. J. Virol. 43, 174-181. 25. Ignoffo, C. M., M. Shapior, and W. F. Hink. 1971. Replication and serial passage of infectious Heliothis nuclear polyhedrosis virus in an establishded line of Heliothis zea cells. J. In vertebr. Pathol. 18:131. 26. Kelly, D. C., D. A. Brown, M. D. Ayres, C. J. Alien, and I. 0. Walker. 1983. Properities of the major nucleocapsid protein of Heliothis zea singly enveloped nuclesr polyhedrosis virus. J. Gen. Virol. 64: 399-408. 27. Langridge, W. H. R. 1981. Biochemical properties of a persistent nonoccluded baculovirus isolated from Heliothis zea cells. Virology. 112,770-774. 28. Lee, J. C., H. H. Chen, H. L. Wei, and Y. C. Chao. 1993. Superinfection induced 15 apoptosis and its correlation of viral progeny in cells persistently infected with Hz-1 baculovirus. J. Virol. 67: 6989-6994. 29. Lee, S. T., S. M. Yu, E. L. Hsu, and Y. C. Chao. 1995. Identification of a very early promoter of insect Hz-1 virus using a novel dual-expression shuttle vector. Nucleic Acids Research 23: 4683-4689. 30. Liao, C. T.,and C. C. Chen. 1998. distribution of Maruca testulalis Geyer eggs and larvae on Sesbania. Bull. Taichung DAIS 59:47-52. 31. Lin, C. H., J. C. Lee, S. S. Chen, H. A. Wood, M. L. Li, C. F. Li, andY. C. Chao. 1999. Persistent Hz-1 virus infection in insect cells: evidence for insertion of viral DNA into host chromosomes and viral infection in a latent status. J. Virol. 73:128-139. 32. Lu, A., and E. B. Carstens. 1991. Nucleotide sequence of a gene essential for viral DNA replication in the baculovirus Autographa californica nuclear polyhedrosis virus. Virology 181: 336-347. 33. Matsumura, S. 1933. Lymantriidae of Japan-Empire. Ins. Matsum. 7:111-152. 34. Miller, D. W. 1988. Genetically engineered viral insecticides, pp. 405-421. "Biotechnology for crop protection" Hedin, P. A., J. J. Menn, and R. M. Hollingworth [eds.]. American Chemical Society. Washington, D. C. 35. Nissen, M. S., and P. D. Friesen. 1989. Molecular analysis of the transcriptional regulatory region of an early baculovirus gene. J. Virol. 63: 493-503. 36. O'Reilly, D. R., L. K. Miller, and V. A. Luckow. 1992. Baculo virus expression vectors. W. H. Freeman and Co., New York, 347pp. 37. Pamela A. Hershberger, J. A. Dickson, and P. D. Friesen. 1992. Site-specific mutagrnesis of the 35-kilodalton protein gene encoded by Autographa californica nuclear polyhedrosis virus: cell line-specific effects on virus replication. J. Virol. 66(9): 5525-5533. 38. Qin, L., Zhang, T., Liu, Y., Madoka, N., Yasuhisa, K. 2002. Fluorescent Brightener 28 Promoting AcMNPV Infection to Spodoptera exigua. Chinese Journal Biological control 18(1):43-44. (In Chinese) 39. Ralston, A. L., Huang, Y., and Kawanishi, C. Y. 1981. Cell culture studies with the IMC-Hz-1 nonoccluded virus. Virology 115:33-44. 40. Rice, W. C., and L. K. Miller. 1986. Baculovirus transcription in the presence of inhibitors and in nonpermissive Drosophila cells. Virus. Res. 6:155-172. 41. Shanma, H. C. 1998. Bionomics, host plant resistance and management of the legume pod borer, Maruca vitrata- a review. Crop Prot. 17:373-386. 42. Theim, S. M., and L. K. Miller. 1989a. Identification, sequence, and transcriptional mapping of the major capsid protein gene of the baculovirus Autographa californica nuclear polyhdrosis virus. J. Virol. 63: 2008-2018. 16 43. Theim, S. M., and L. K. Miller. 1989b. A baculovirus gene with a novel transcription pattern encodes a polypeptide with a zinc finger and a leucine zipper. J. Virol. 63: 4489-4497. 44. Tomalski, M. D., J. Wu. and L. K. Miller. 1988. The location, sequence, transcription and regulation of a baculovirus DNA polymerase gene. Virology 167: 591-600. 45. Vail, P. V., D. L. Jay, and W. F. Hink. 1973. Replication and infectivity of the nuclear polyhedrosis virus of the alfafa looper, Autographa californica, produced in cells grown in vitro. J. Invertebr. Pathol. 22:231. 46. Volkman, L. E., G. W. Blissard, P. Friesen, B. A. Keddie, R. Possee, and D. A. Theilmann. 1995. Virus Taxonomy: The classification and Nomenclature of Viruses. In: Sixth Report of the International Committee on Taxonomy of Viruses (Murphy, F. A., et al., eds), pp. 104-113. Springer, New York. 47. Wilson, M. E., T. H. Mainprize, P. D. Friesen, and L. K. Miller. 1987. Location, transcription and sequence of a baculovirus gene encoding a small arginine-rich polypeptide. J. Virol. 61: 661-666. 48. Wood, H. A. and J. P. Burand. 1986. Persistent and productive infections with the Hz-1 baculovirus, pi 19-134. In Current Topics in Microbiology and Immunology: The Molecular Biology of Baculovirus. Doerfler, W. and P. Bohm eds. Spring-Verlag, Berlin. 49. Yu, C. C., H. H. Kao, J. T. Chao, S. S. Lu, and C. H. Wang. 1997.The characterization of Lymantria xylina nucleopolyhedrovirus(LyxyNPV)and the estabishment of in vitro multiplication of LyxyNPV. Chinese. J. Entomol. 17(1): 23-32. (In Chinese) 17