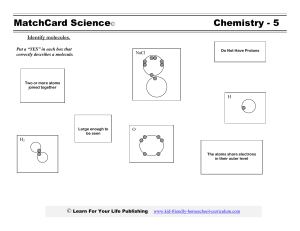
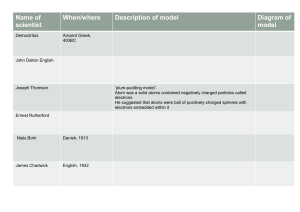
2اسئلة محاضرة اهم النقاط التي أكدت عليها نظرية Dalton’s Atomic Theory Experiment is aimed to تركيز A. Elements are composed of extremely small particles called atoms تتكون .العناصر من جسيمات صغيرة للغاية تسمى الذرات B. The atom must also contain positive particles that balance exactly the negative charge carried by particles that we now call electrons ضا على جسيمات موجبة توازن تما ًما ً يجب أن تحتوي الذرة أي الشحنة السالبة التي تحملها الجسيمات التي نسميها اآلن اإللكتر C. Cathode rays are stream of tiny particles a negative electrical charge, called electrons أشعة الكاثود عبارة عن تيار من جسيمات صغيرة شحنة كهربائية سالبة تسمى اإللكترونات 2 تركيز J. J. Thomson Experiment is aimed to ........ A. Determined the charge-to-mass ratio of an electron.تحديدشحنة االلكترون الى كتلة االلكترون B. Elements are composed of extremely small particles called atoms تتكون العناصر من جسيمات C. The atom must also contain positive particles that balance exactly the negative charge carried by particles that we now call electrons يجب أن تحتوي الذرة ضا على جسيمات موجبة توازن تما ًما الشحنة السالبة التي تحملها الجسيمات التي ً أي نسميها اآلن اإللكتر D. Cathode rays are stream of tiny particles a negative electrical charge, called electrons أشعة الكاثود عبارة عن تيار من جسيمات صغيرة شحنة كهربائية سالبة تسمى اإللكترونات 3 تركيز ماهى الغاية من اجراء تجربة Rutherford’s Experimentis aimed to A. Determined an electron.تحديد االلكترون B. Elements are composed of extremely small particles called atoms تتكون العناصر من جسيمات C. The Discovery of the Nucleus اكتشاف النواة D. Cathode rays are emitted by the negatively charged electrode (cathode) أشعة الكاثود عبارة عن تيار من جسيمات صغيرة شحنة كهربائية سالبة تسمى اإللكترونات 4 A. مالحظة تركيز من مالحظة النموذج السابق نالحظ أن From this model we can obsarve that A. Electron number didn’t equal protons number. عدد االلكترونات ال تساوى عدد البروتونات B. The nucleus is positively chargedالنواة موجبة الشحنة C. The Discovery of the Nucleus اكتشاف النواة D. The nucleus is negative chargedhالنواة سالبة الشحنة 5 A. تذكر Mass of atom expressed in 6 A. Protons B. Neutrons C. Electrons D. Atomic mass unit Mass of atom expressed in A. number of protons in nucleus+ number of Electrons B. number of protons + number of neutrons C. Electrons D. number of protons in nucleus The numper 23 in sodiuom refers to Mass number 23 B. Neutrons number 11 C. Electrons number D. Atomic number A. 7 Na identity Chemical Symbol of Sodium is 8 A. Au B. Cl C. Na D. Ne Symbol Name of the element writing with One capital letter is A. Oxygen B. Sodium C. Chlorine D. Gold تحليل How many neutrons are in an atom of 9 A. 52 B. 24 C. 76 D. 28 Number of protons = A. Number of neutron + Number of protons Chlorine B. Number of neutron C. Number of electrons D. Number of neutron + Atomic number How many protons, electrons, are in an atom of A. 11 23 Na 11 10 B. 23 C. 12 D. 34 تحليل Mass Number of 11 A. 27 B. 14 C. 13 D. 40 Number of p, e and n in Atoms Protons Neutrons 6 7 Electrons Atomic Number 42 96 55 12 Mass Number 133 Atomic Symbol Which of the following elements is a metal? a. Sb b. O c. Br d. Ag Which of the following elements is a noble gas? a. As b. C c. F d. Co e. He Sodium belongs to the ________ group of the periodic table تصنيف. a. alkali metal b. transition element c. noble gas d. nonmetal How many electrons does the Se2– ion possess? a. 32 b. 36 c. 4 d. 0 e. 34 Identify the cation. a. O2– b. Sr2+ c. Br d. Kr e. I2 17 1) Isotopes differ in the number of a. gamma particles. b. electrons. c. compounds. d. neutrons. Calculate number of moles of 1.1 × 1022 silver atoms? a. 4.52 × 1024 atoms b. 1.52 × 1024 atoms c. 4.8266 × 10-2 atoms d. 3.01 × 1024 atoms e. 1.8266 × 10-2 atoms 19 Calculate number of moles of 1.1 × 1022 silver atoms? a. 4.52 × 1024 atoms b. 1.52 × 1024 atoms c. 4.8266 × 10-2 atoms d. 3.01 × 1024 atoms e. 1.8266 × 10-2 atoms 20 Calculate the number of atoms in 2.45 mol of Cu a. 4.52 × 1024 atoms b. 1.48× 1024 atoms c. 2.94 × 1022atoms d. 3.01 × 1024 atoms e. 2.94 × 1023 atoms 21 Calculate the moles of 0.0265 g of Carbon a. 4.52 × 1024 atoms b. 1.48× 1024 atoms c. 2.94 × 1022atoms d. 3.01 × 1024 atoms e. 2.21 × 10-3 atoms 22 Calculate the moles of 0.0265 g of Carbon. Given: 0.0265 g C Relationships: 1 mol C = 12.01 g Solution: 23